Novo Nordisk käynnisti 5. heinäkuuta Kiinassa CagriSema-injektion kliinisen vaiheen III tutkimuksen, jonka tarkoituksena on verrata CagriSema-injektion turvallisuutta ja tehoa semeglutidiin lihavilla ja ylipainoisilla potilailla Kiinassa.
CagriSema-injektio on Novo Nordiskin kehittämä pitkävaikutteinen yhdistelmähoito, jonka pääkomponentit ovat GLP-1 (glukagonin kaltainen peptidi-1) -reseptoriagonisti smeglutidi ja pitkävaikutteinen amyliinianalogi kagrilintidi.CagriSema-injektio voidaan antaa ihon alle kerran viikossa.
Ensisijaisena tavoitteena oli verrata CagriSemaa (2,4 mg/2,4 mg) semeglutidiin tai lumelääkkeeseen kerran viikossa ihon alle.Novo Nordisk on julkistanut tulokset vaiheen 2 diabeteksen hoitoon tarkoitetusta CagriSema-tutkimuksesta, joka osoitti, että CagriSeman hypoglykeeminen vaikutus on parempi kuin semeglutidilla, ja lähes 90 % tutkittavista on saavuttanut HbA1c-tavoitteen.
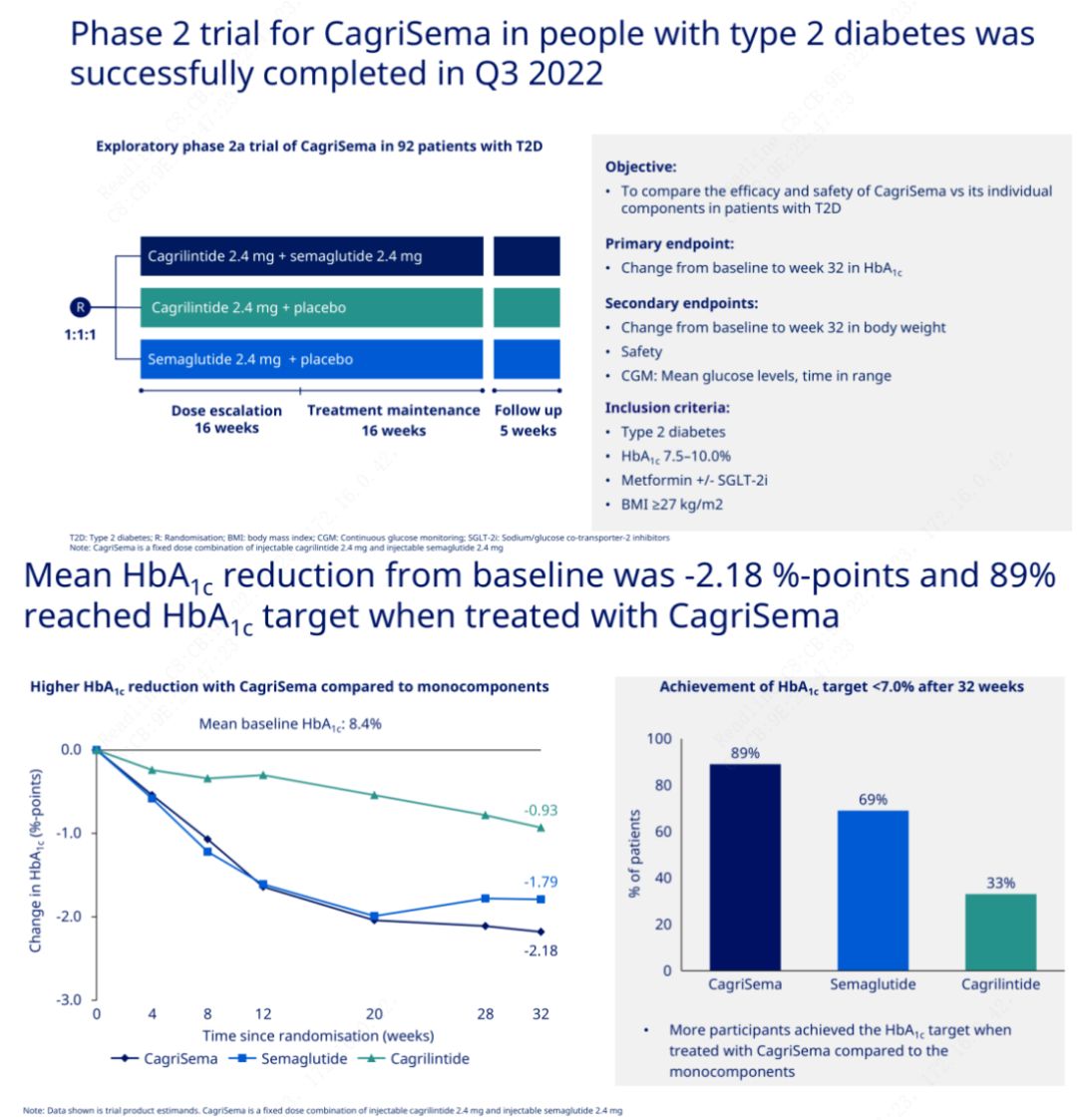
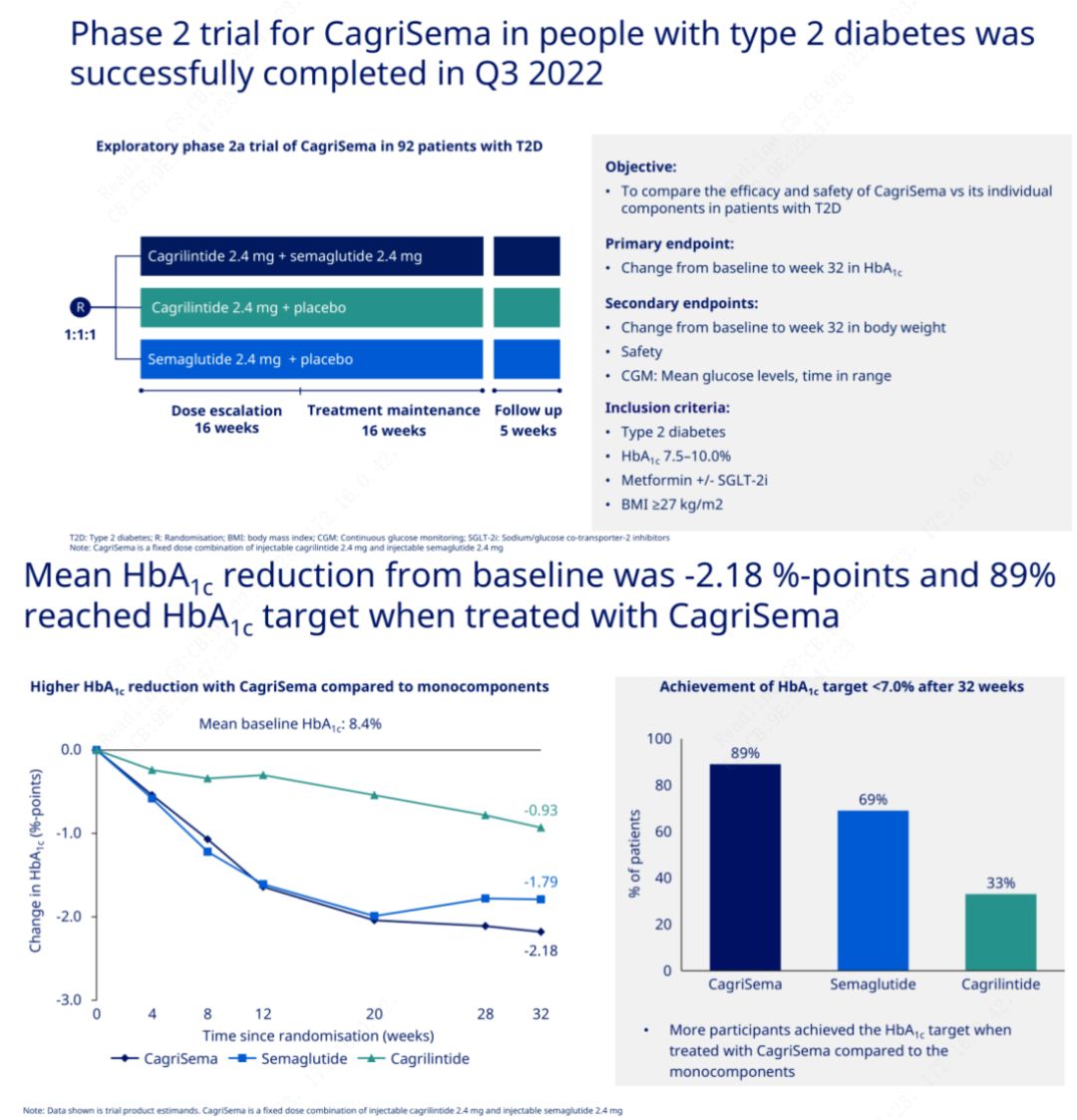
Tiedot osoittivat, että merkittävän hypoglykeemisen vaikutuksen lisäksi CagriSema-injektio ylitti merkittävästi semeglutidin (5,1 %) ja kagrilintidin (8,1 %) painonpudotuksen ollessa 15,6 %.
Innovatiivinen lääke Tirzepatidi on maailman ensimmäinen hyväksytty viikoittainen GIP/GLP-1-reseptoriagonisti.Se yhdistää kahden inkretiinin vaikutukset yhdeksi molekyyliksi, joka ruiskutetaan kerran viikossa ja on uusi tyypin 2 diabeteksen hoitomuoto.Yhdysvaltain elintarvike- ja lääkevirasto (FDA) hyväksyi tirtsepatidin toukokuussa 2022 parantamaan sokeritasapainoa (ruokavalion ja liikunnan perusteella) tyypin 2 diabetesta sairastavilla aikuisilla, ja se on tällä hetkellä hyväksytty Euroopan unionissa, Japanissa ja muissa maissa.
Eli Lilly julkisti 5. heinäkuuta vaiheen III SURPASS-CN-MONO -tutkimuksen lääketutkimuksen kliinisten tutkimusten rekisteröinti- ja tiedonantoalustasta tyypin 2 diabetespotilaiden hoitoon.SURPASS-CN-MONO on satunnaistettu, kaksoissokkoutettu, lumekontrolloitu vaiheen III tutkimus, jonka tarkoituksena on arvioida tirtsepatidimonoterapian tehoa ja turvallisuutta lumelääkkeeseen verrattuna tyypin 2 diabeetikoilla.Tutkimukseen suunniteltiin 200 tyypin 2 diabetesta sairastavaa potilasta, jotka eivät käyttäneet mitään diabeteslääkkeitä 90 päivää ennen käyntiä 1 (paitsi tietyissä kliinisissä tilanteissa, kuten akuutti sairaus, sairaalahoito tai elektiivinen leikkaus, lyhytaikainen (≤14). päivää) insuliinin käyttö).
Tyypin 2 diabeteksen odotetaan hyväksyvän tänä vuonna
Viime kuussa SURPASS-AP-Combo-tutkimuksen tulokset julkaistiin 25. toukokuuta menestyslehdessä Nature Medicine.Tulokset osoittivat, että glargininsuliiniin verrattuna Tirzepatide osoitti paremman HbA1c:n ja painon alenemisen tyypin 2 diabetespotilaiden populaatiossa Aasian ja Tyynenmeren alueella (pääasiassa Kiinassa): HbA1c:n lasku jopa 2,49 % ja painon lasku jopa 7,2 kg. (9,4 %) 40 hoitoviikon kohdalla veren lipidien ja verenpaineen merkittävä paraneminen sekä yleinen turvallisuus ja siedettävyys olivat hyviä.
SURPASS-AP-Combon faasin 3 kliininen tutkimus on Tirzepatiden ensimmäinen tutkimus, joka suoritettiin pääasiassa kiinalaisilla tyypin 2 diabetespotilailla ja jota johti professori Ji Linong Pekingin yliopistollisesta kansansairaalasta.SURPASS-AP-Combo on yhdenmukainen maailmanlaajuisen SURPASS-tutkimussarjan tulosten kanssa, mikä edelleen todistaa, että kiinalaisten potilaiden diabeteksen patofysiologia on yhdenmukainen maailmanlaajuisten potilaiden patofysiologian kanssa, mikä on perusta uusien lääkkeiden samanaikaiselle tutkimukselle ja kehittämiselle. Kiinassa ja maailmassa, ja se tarjoaa myös vankkaa näyttöä siitä, että kiinalaisille potilaille annetaan mahdollisuus käyttää uusimpia diabeteksen hoitoon tarkoitettuja lääkkeitä ja niiden kliinistä käyttöä Kiinassa mahdollisimman pian.
Postitusaika: 18.9.2023

